Химия
Тема 1: Краткий курс химииУрок 2: Химические элементы и вещества в свете электронной теории. Химическая связь
- Теория
Химическая связь — это силы взаимодействия между атомами или группами атомов, приводящие к образованию молекул, ионов, свободных радикалов, а также ионных, атомных и металлических кристаллических решеток.
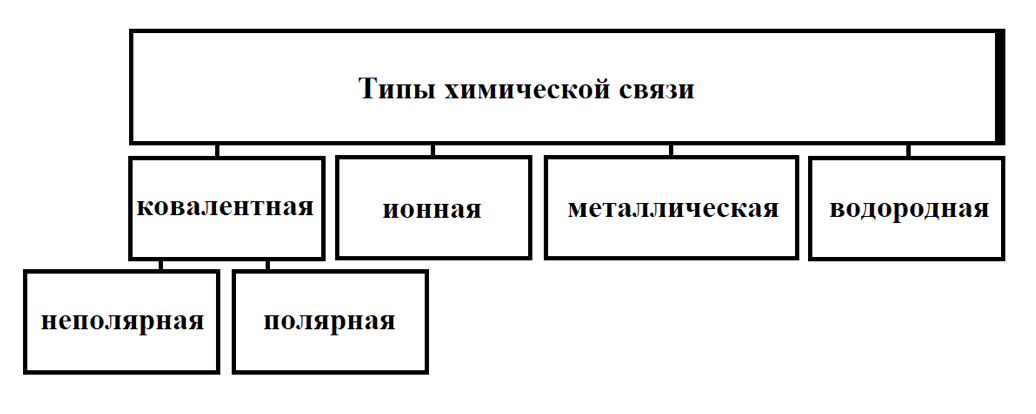
Различают четыре основных типа химической связи:
Ковалентная связь – это связь, которая образуется между атомами с одинаковой электроотрицательностью или между атомами с небольшой разницей в значениях электроотрицательности.
При образовании химической связи между атомами главную роль играют их ВАЛЕНТНЫЕ ЭЛЕКТРОНЫ, наименее прочно связанные с ядром атома. Все атомы при образовании молекул стремятся приобрести устойчивую восьмиэлектронную (октет) – как у инертных газов - или двухэлектронную оболочку (дублет) оболочку.
Рассмотрим теорию ковалентной связи на примере образования простейшей молекулы – молекулы водорода Н2.

У атомов водорода внешний энергетический уровень является незавершённым (электронная формула атома водорода 1s1). Для завершения энергетического уровня до устойчивой конфигурации инертного газа (двухэлектронной оболочки Не) каждому атому водорода не хватает по одному электрону. При взаимодействии двух атомов водорода происходит спаривание двух электронов с противоположными спинами и формирование общей электронной пары. Такое «упорядочивание» неспаренных электронов протекает с выделением энергии, т. е. при взаимодействии атомов общая энергия системы понижается и это является признаком образования химической связи. В молекуле водорода - ковалентная неполярная связь.
При перекрывании s-орбиталей атомов водорода повышенная электронная плотность создаётся между ядрами атомов и электроны испытывают притяжение сразу двух ядер, что способствует образованию прочной связи: Согласно теории Электронной структуры атомов, атомы химических элементов в молекулах стремятся получить стабильную электронную конфигурацию ближайшего инертного газа. Например, при слиянии атомов фтора в молекулу образуется конфигурация неона:

Ковалентная неполярная связь образуется между атомами одинаковых элементов – неметаллов. Значит, это простые вещества неметаллы - H2, N2, O2, F2, Cl2, Br2, I2. В зависимости от числа общих электронных пар между атомами в молекулах с КНС существуют одинарные (как в водороде и галогенах), так и двойные – в молекуле кислорода, и тройные – в молекуле азота связи.

Ковалентная полярная связь возникает между атомами с разной электроотрицательностью (как правило, разными неметаллами) и характеризуется смещением общей электронной пары к более электроотрицательному атому (поляризацией).
Большую часть времени обобществленые электроны находятся ближе к одному атому, чем к другому. Примером ковалентной полярной связи могут служить связи, возникающие в молекуле фтороводорода, там обобществленые электроны, ответственные за образование ковалентной связи располагаются ближе к атому фтора, нежели водорода. Все дело в том, что электроотрицательность у фтора больше чем у водорода.

Ковалентная связь классифицируется по механизмам образования: обменный механизм (за счёт общих электронных пар); донорно-акцепторный (атом - донор обладает свободной электронной парой и передаёт её в общее пользование с другим атомом - акцептором, у которого имеется свободная орбиталь).
Донорно-акцeпторная связь:

Донорно-акцeпторная связь отличается только способом образования; по свойствам она одинакова с остальными ковалентными связями.
Список веществ, образованных по донорно-акцепторному механизму:
NH4+ - ион аммония
NO3- - нитрат ион
O3 - озон
H3O+ - ион гидроксония
CO - угарный газ
K[Al(OH)4], Na2[Zn(OH)4] - во всех комплексных солях есть хотя бы одна ковалентная связь, возникшая по донорно-акцепторному механизму.
Ионная связь - один из видов химической связи, в основе которого лежит электростатическое взаимодействие между противоположно заряженными ионами. Ионы образовались в результате полного перехода общей электронной пары к атому с большей электроотрицательностью.

В наиболее частом случае ионная связь образуется между типичным металлом и типичным неметаллом (ЭО >1,7). Примеры: NaF, CaCl2, MgF2, Li2S, BaO, RbI.
*** Существуют вещества, молекулы которых содержат и ионные, и ковалентные связи. Это щелочи и многие соли. Например, в гидроксиде натрия NaOH связи между атомами натрия и кислорода – ионные, а между атомами кислорода и водорода – ковалентные полярные.
Металлическая связь - вид химической связи, удерживающей вместе атомы металла. Этот тип связи выделен отдельно, так как его отличием является наличие высокой концентрации в металлах электронов проводимости - "электронного газа". Атомы металлов достаточно легко отдают валентные электроны, превращаясь при этом в катионы. Металлическая связь - это связь между атомами, ионами и свободными электронами в общем кристалле металла.
Схема металлической связи:

"Облако" электронов в металлах способно приходить в движение под различным воздействием. Именно оно является причиной электропроводности и некоторых других свойств металлов и сплавов.
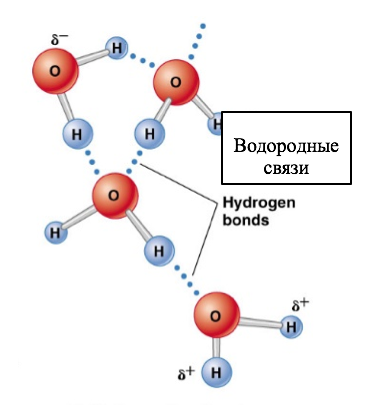
Водородная связь - это межмолекулярные (или внутримолекулярные) химические связи, возникающие между молекулами, в которых есть сильно полярные ковалентные связи — H-F, H-O, H-S или H-N. Если в молекуле есть такие связи, то между молекулами будут возникать дополнительные силы притяжения.
Водородные связи - очень слабые связи ~ в 10 раз слабее ковалентной.
НО! Благодаря водородным связям вода – жидкость при обычных на Земле температурах (сравн. с H2S, CH4, NH3)
Одна из наиболее частых ошибок считать, что в самом газе, водороде, имеются водородные связи - это вовсе не так.
Они имеются между молекулами:
- H2O
- NH3
- HF
- Органических спиртов: С2H5OH, C3H7OH
- Органических кислот: CH3COOH, C2H5COOH
Водородные связи:
Алгоритм определения типа химической связи в веществах: